K8凯发官网我们身体里的各个类型的细胞就像一个个训练有素的工人——皮肤细胞负责屏障、肝细负责代谢和解毒、脑细胞负责思考...它们各司其职,维持者身体的健康运转。这些细胞和组织身份的丧失,是衰老和多种疾病的标志性特征,但其潜在机制,目前尚不明确。
该研究表明,随着年龄增长或疾病侵袭,越来越多的细胞开始“迷失”自己的身份,丢掉了“专业技能”,变得“不务正业”,甚至开始搞破坏,研究团队将这种现象称为——“间充质漂移”(Mesenchymal Drift,MD),更令人振奋的是,研究团队找到了逆转这一状态的方法——部分重编程!这项研究从机制层面揭示了部分重编程的潜在有益效应,并为开发基于部分重编程手段逆转衰老及衰老相关疾病的干预策略提供了理论框架。

衰老细胞的表观遗传图谱显示其维持细胞身份的能力减弱。之前的研究发现,处于复制性衰老的细胞表现出类似于成纤维细胞向肌成纤维细胞转变(FMT)的特征。这些研究表明,在衰老过程中细胞状态可能会发生潜在转变,通常还伴随着各种分子特征的变化。
2006 年,山中伸弥教授发现,过表达四种转录因子——山中因子(OCT4、SOX2、KLF4 和 MYC,简称为 OSKM),能够将完全分化的体细胞重编程为多能状态,即人工诱导多能干细胞(iPSC),山中伸弥也因这一贡献而获得了 2012 年诺贝尔生理学或医学奖。
基于 OSKM 的细胞重编程技术已成为一种很有前景的方法,能够恢复衰老相关表型,其在体外和体内均显示出有效性。然而,这种返老还童效应的确切机制,仍不完全清楚。
通过 OSKM 对成纤维细胞进行的完全重编程以进入多能状态,始于一个被称为间充质-上皮转化(MET)的过程,在此过程中,细胞从间充质状态去分化为上皮状态。这也引发了一个令人深思的问题——这种细胞状态的转变对于返老还童来说是否是必不可少的,还是说它只是是重编程过程中一种潜在的有害副产品,应当加以避免?
间充质漂移(MD)的增强与疾病进展、患者生存率降低及死亡风险升高相关,而抑制关键 MD 转录因子可引发表观遗传年轻化。值得注意的是,山中因子(OSKM)诱导的部分重编程能够在细胞去分化和获得多能性之前显著降低间充质漂移,并在细胞与组织层面实现衰老转录组的返老还童。
研究团队对来自 40 余种人体组织和 20 种衰老性感疾病(肺纤维化、阿尔茨海默病、慢性肾病、脂肪肝等)的基因表达数据进行分析,结果显示,随着年龄增长或疾病发生,多种类型的细胞都开始上调一组与“间充质状态”相关的基因,且间充质细胞群的数量也在增加,也就是细胞变得更具活动性、能产生大量纤维结缔组织和炎症因子的状态,表明在细胞和组织层面都出现了向间充质身份的转变。这就像原本负责特定工作的细胞开始“漂移”身份,变得像成纤维细胞或肌成纤维细胞。研究团队将这种现象称为——间充质漂移(Mesenchymal drift,MD)。
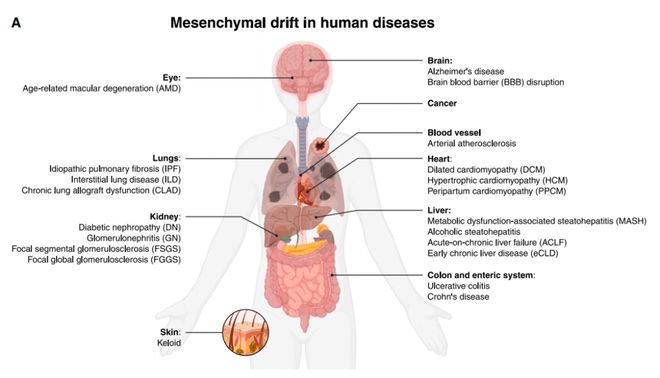
研究团队还开发了一个衡量“间充质漂移”程度的指标,这个指标强烈预示着疾病的严重程度、患者生存率的降低和死亡风险的增加!例如,在致命性的特发性肺纤维化(IPF)患者中,间充质漂移程度高的患者生存期显著缩短。
1、器官功能丧失:肺泡细胞“漂移”了,肺就不能有效交换气体;肝细胞“漂移”了,肝脏的解毒和代谢功能就受损;肾小管细胞“漂移”了,肾脏的过滤功能就下降。
2、组织纤维化:大量细胞产生异常的细胞外基质,导致组织变硬、失去弹性,这正是肺纤维化、肝硬化的核心特征。
3、慢性炎症:处于“漂移”状态的细胞会释放更多促炎因子,形成一个持续的、低度的炎症环境(炎性衰老),进一步损害组织并加速衰老。
4、系统性问题:血液中一些促进这种“漂移”的信号分子(例如 TGF-β 超家族成员)在衰老过程中显著升高,且这些分子本身也与死亡风险高度相关。这意味着某个器官的“漂移”可能通过血液信号影响到全身。
既然“间充质漂移”是衰老和多种疾病的共同核心机制,那能否逆转这一过程呢?
研究团队将目光投向了曾获诺奖的“细胞重编程”技术——使用山中因子 OCT4、SOX2、KLF4、MYC(OSKM)。但完全逆转成干细胞可能存在导致肿瘤的风险,关键在于“恰到好处”——部分重编程(Partial Reprogramming)。
研究团队使用山中因子对来自 96 岁老人的皮肤细胞进行了重编程,并利用单细胞测序技术,追踪了重编程过程中基因表达变化情况。结果发现,在细胞真正开始向干细胞逆转之前,有一个短暂的“部分重编程”阶段。在这个阶段,驱动“间充质漂移”的关键基因(例如 SNAI1、TWIST1、ZEB1、ZEB2)和促纤维化的 TGF-β 信号被迅速且显著地抑制了。同时,这些衰老细胞的整体基因表达谱也神奇地向年轻状态逆转!而那些没有进入这个“部分重编程”路径的细胞,则依然保持着衰老和“漂移”的特征。
研究团队进一步比较了年轻和年老细胞的反应,发现年轻细胞更容易被山中因子完全重编程为干细胞,但山中因子对抑制年老细胞中过度的“间充质漂移”更为有效。这提示部分重编程可能对衰老细胞有独特的“纠偏”作用。
更重要的是,研究团队使用一个不能诱导干细胞形成、但能启动重编程早期过程的 OCT4 突变体,也能有效地抑制“漂移”基因并让细胞变年轻。这证明抑制“漂移”本身可能就是重编程发挥“返老还童”作用的关键机制之一,不一定非要完全重编程到干细胞那一步。
研究团队回顾和分析了多项已发表的动物实验数据,这些实验采用了不同的部分重编程策略,例如周期性诱导山中因子或仅在特定衰老细胞中诱导部分山中因子,结果显示,在自然衰老或早衰的小鼠中,进行部分重编程(几周到数月)后,在容易出现纤维化的器官(例如肝脏和肾脏)中检测到了显著的“间充质漂移”基因表达的降低。在脾脏、皮肤、骨髓等组织中也观察到了下降趋势。
这些动物实验同时还观察到,部分重编程能减轻组织纤维化、改善器官功能、延长健康寿命甚至整体寿命。例如,在肠道中,部分重编程能降低多种肠上皮细胞的“间充质漂移”水平,促进损伤后修复;在骨髓中,能够改善造血干细胞功能和减少炎症。
这些结果表明,部分重编程能够逆转衰老器官的“间充质漂移”,恢复组织健康,甚至延长寿命和健康寿命。
总的来说,这项研究具有里程碑意义,它揭示了“间充质漂移”是跨越多种组织和疾病的、普遍存在的衰老核心特征之一,为理解衰老和年龄相关疾病的共同病理基础提供了统一机制和全新框架;提出了“间充质漂移”是干预衰老和多种衰老相关疾病的一个极具前景的核心靶点;阐明了部分重编程为何能够实现“返老还童”的关键机制——触发一个早期、短暂的重编程过程,优先纠正细胞身份的“迷失”,抑制促纤维化、促炎状态,让细胞恢复更年轻、更“专业”的功能状态,而非一定要变成干细胞。
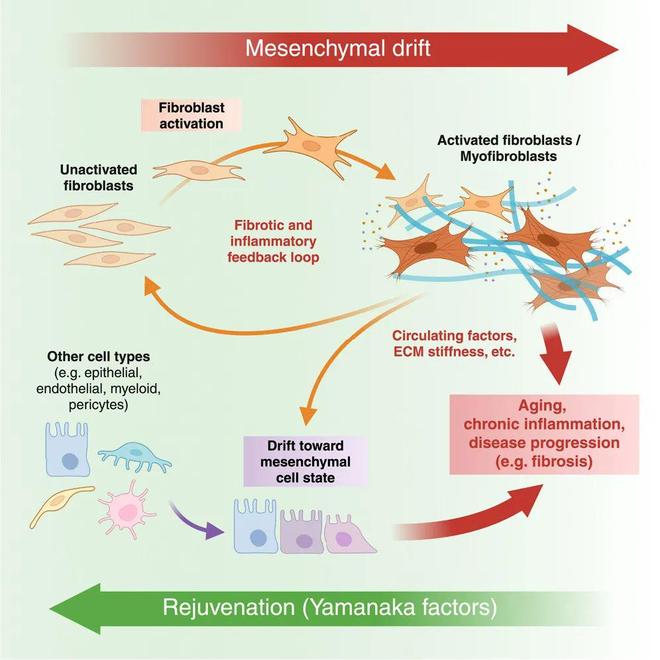
细胞的身份“迷失”——“间充质漂移”,是潜伏在时光流逝和众多疾病背后的隐秘推手。这项突破性研究不仅为我们揭开了这层面纱,更点亮了一盏逆转的明灯——部分重编程。它就像一个精准的“时光橡皮擦”,在细胞完全“返老还童”成干细胞之前,巧妙地擦除了它们“转行”的错误印记,帮助它们找回“初心”和“专业技能”。这些发现为开发逆转衰老相关功能下降、治疗纤维化疾病甚至神经退行性疾病的全新策略指明了方向,未来还可能开发出模拟部分重编程效应、更精准靶向“间充质漂移”的药物或疗法。

2022 年 1 月,Altos Labs携30 亿美元巨额融资走出隐身模式,这也是生命科学领域有史以来规模最大的一笔融资。投资人包括亚马逊创始人、世界首富贝索斯,以及脸书早期投资人 Yuri Milner 等人。该公司创始团队阵容强大,科学家团队同样耀眼,4位诺奖得主作为高级科学顾问或董事会成员加入,还有多位抗衰老领域顶尖学者加盟。
Altos Labs 的长期计划是通过生物重编程技术使细胞重新恢复活力,进而扩展到动物乃至人类,最终实现逆转衰老、延长人类寿命的理想。
该公司也表示,其短期目标并不包括盈利,目前将致力于在科学上取得突破,通过破解细胞再生的奥秘,来逆转导致伤害和残疾的疾病和衰老过程,以创造一种全新的医学方法,安全有效地重编程细胞,为未来医学开辟新的前景。成立以来,Altos Labs 的研究人员已发表多篇重磅研究论文。

